Općenito o radioaktivnog raspada i ionizirajućeg zračenja
Moderna fizika je otvorio širok spektar primjene nuklearne energije u medicini. Za liječnici postali dostupni korištenje radioaktivnih izotopa raznih kemijskih elemenata, koji su već znatno proširena istraživanja, dijagnostičke mogućnosti i terapijsku primjenu ionizirajućeg zračenja.Trenutno, teško je zamisliti kako široko u budućnosti će se koristiti ionizirajućeg zračenja u medicinskoj praksi. Stoga je sasvim razumljivo zanimanje za biološke učinke različitih vrsta ionizirajućeg zračenja.
Uspjesi fizike i otkrića u drugim područjima znanosti koji su obilježili kraj XIX stoljeća, pomogao otkriti „tajne” o blagotvornim učincima mnogih voda istochnikov- radioaktivni izotopi su otkrivena u njima. Kao što je prikazano daljnjim istraživanjima, glavni izotopi koji se nalaze u radioaktivnih voda su radon i proizvodi njegovog raspadanja.
Ovdje su najčešći obrasci radioaktivnog raspada radona vodama i prateće ionizirajućeg zračenja, vjerujući da će to biti korisno širokom krugu čitatelja zainteresiranih za medicinsku upotrebu tih voda.
Godine 1896. Becquere otkrio da uran emitira zrake, djeluje na fotografske ploče i mogućnosti ionizirati zrak. Nekretnine izotopi koji se spontano emitiraju nevidljive zrake Pierre i Marie Curie je nazvana radioaktivnost. Oni otvoren u 1898, radioaktivnost radija i polonija, Schmidt - radioaktivnosti torij.
Počelo je široki pojas novih otkrića. Rutherford (1902) je utvrdio da radioaktivni raspad je povezana s tri vrste zračenja, koje je nazvao prvih grčkih slova abecede (A, (B- i y-zrake)). Ove emisije su različite u svojoj fizičkoj prirodi i imaju različite propuštanje i ionizirajuće sposobnosti.
Testovi u magnetskom polju pokazali su da alfa čestice pozitivno nabijeni u čestica - negativnog naboja, a zadužen čestice nema. Biološki učinak A-, B- i y-zračenja na organizam i njegovih različitih fizioloških sustava.
Radioaktivni i ne-radioaktivni izotopi - kemijskih elemenata atoma vrste različite jedna od druge njihove mase. Kemijska svojstva izotopa istog elementa su gotovo identični, ali njihovo fizičko i, posebice, radioaktivni svojstva različita. Neki izotopi se nalaze u prirodnom usloviyah- mnogo više da bi ih se kroz laboratoriju.
fizičar DD Ivanenko struktura jezgre predlaže teoriju, prema kojoj se jezgra sastoji od elementarnih čestica - protona i neutrona. Ove čestice su gotovo jednake mase, međutim, pozitivno nabijene protone i neutrone ne nose naboj.
Daljnje studije pokazale su da isti kemijski element ima atoma koji su u središtu isti broj protona i elektrona sadrže različit broj neutrona. Takvi atomi su isti kemijska svojstva, ali različita fizikalna svojstva. To je izotopi kemijskih elemenata.
Tako, na primjer, vodikov ima dva stabilna nisu radioaktivni izotop - laki i teški vodik vodik - deuterij. U svjetlu vodika jezgre sastoji se od samo jednog protona, u teški - jedan proton i jedan neutrona.
Fizikalna svojstva izotopa kemijskih elemenata mogu biti radioaktivna neradioaktivnog stabilan.
Radioaktivni izotopi karakterizira nestabilnosti njihovih jezgara, te prijelaz na stabilniji stanja popraćena ionizirajućeg zračenja.
U prirodi postoje tri poznata roditelj radioaktivni izotop - uran, torij i aktinium-urana. Svaki od tih izotopa u procesu radioaktivnog raspada se prevesti u druge kemijske supstance, naznačen time, da je konačni stabilni produkt razgradnje je jedan od ne-radioaktivnih izotopa olova.
U sva tri obitelji jednog od radioaktivnog raspada radioaktivnog plina koji se zove emanacija. Među urana - radij zračenje je radon, torij - emanacija torij (thoron), aktin-uranij - actinon. Uz daljnje propadanje emanacije opet pretvoriti u metalima.
Neka nam vidjeti kako radioaktivnog raspada izotopa nizu urana - radija, uz najvažnije u medicinskoj praksi.
Urana (U238) - radioaktivni kemijski element, čiji je maseni broj jednak 238, široko je rasprostranjen u Zemljinoj kori. Uranij - srebrni metal, ima visoku kemijsku aktivnost. Fizikalna svojstva alfa je aktivni element s poluživotom 4,5-10-9 godina. Urana yavlyaetcya predak radioaktivnog radij obitelji.
Radij (Ra226) otvorena je 1898. godine, Marie Curie-Sklodowska i Pierre Curie kao propadanja proizvod urana. Radij - zemnoalkalijski metal, koja je jednaka masenom broju 226 i pol života je 1620 godine. Radioaktivni raspad radij popraćena a i y-zračenje. U medicinskoj praksi, kao i za radona uobičajeno koriste klor, brom radij soli koje su lako topljive u vodi.
Radij, kao i uran, su široko rasprostranjeni u prirodi - u stijenama, prirodne vode, kao iu tijelu biljke, životinje i ljude. Maksimalno dopuštena koncentracija radija u kućanstvu pitke vode ne smije biti veća od 5.10.11 Ci / l. Radij u postupku raspada u radon transformacije (Rn222) (radij zračenje).
Radon (Rn222) - plin, radioaktivni kemijski element-je otvoren u 1900, fizičar E. Rutherford i E. Dorn i gotovo istovremeno Debvernom. Masa broj 222 je jednaka radona i njegove punjenja jezgre 86. radon-222 - inertnog plina, koji je također izložen daljnje transformacije, uz zračenjem.
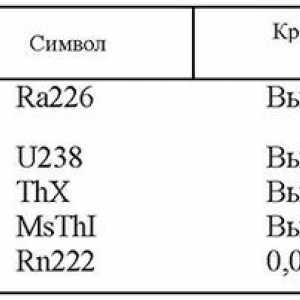
Radon oblikovan direktno iz radija. To je široko distribuiran u prirodi - u zraku, minerala i pitke vode i tla. U procesu raspada radona emitiraju alfa čestice, on se pretvara u kratkotrajno izotop - radij A, čime se popeti na grupu tzv radona potomstva, koje su veće ili manje količine su gotovo uvijek tamo, gdje se nalazi radon. Ovdje je kratak opis radioaktivnih izotopa koji su u radon vodama (Tablica 2.).
Tablica 2. Karakteristike radioaktivnih izotopa


Proces radioaktivnog raspada i stvaranja novih kemijskih tvari podliježe određenom zakonom. U isto vrijeme, u razdoblju od radioaktivnog raspada svakog izotopa - konstanta.
Vrijeme potrebno za pola raspadanja radioaktivnih izotopa atoma, i stalni zove poluživot. Za svaki izotop ovaj put razlikuje, ona se razlikuje od milijardi godina (npr U238) u frakcijama sekundi (C1 radija). Za radona (Rn222) poluraspada je 3.825 dana.
Radijusi A, B radij, radij C i radij C1 zovu kratkotrajni kćeri radona propadanja proizvoda. Kao rezultat toga, oni postaju otporniji radij D (Ra D210), vrijeme poluraspada je 23,3 godina.
Ovisna proizvodi radona, kao metal, položeno na površinu s kojom dolaze u kontakt. To čini aktivni sloj, naznačen time, da je daljnji radioaktivnog raspada.
EA Smirnov-Kamensky, SM petelin
Dijelite na društvenim mrežama:
Povezan
 Bolest uzrokuje zračenje, simptome, dijagnostici i liječenju bolesti zračenja
Bolest uzrokuje zračenje, simptome, dijagnostici i liječenju bolesti zračenja Znanstvenici su izmislili tabletu protiv zračenja
Znanstvenici su izmislili tabletu protiv zračenja Suhe šljive štite kosti od zračenja
Suhe šljive štite kosti od zračenja Profesionalne bolesti gornjeg dišnog sustava
Profesionalne bolesti gornjeg dišnog sustava Pomoć sa kombiniranim ozljede zračenja u fazama medicinske evakuacije
Pomoć sa kombiniranim ozljede zračenja u fazama medicinske evakuacije Čimbenici koji utječu na nuklearno oružje
Čimbenici koji utječu na nuklearno oružje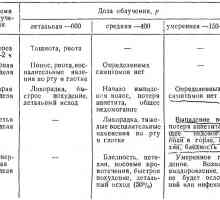 Bolesti zračenje u kombinaciji lezija
Bolesti zračenje u kombinaciji lezija Balneoterapija u rehabilitaciji srčanih bolesnika
Balneoterapija u rehabilitaciji srčanih bolesnika Broj i vrijeme prijema na radon pitke
Broj i vrijeme prijema na radon pitke Složena radon
Složena radon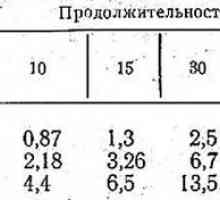 Dozimetrijski karakteristike izlaganja inhalacijom zraka obogaćeni radona
Dozimetrijski karakteristike izlaganja inhalacijom zraka obogaćeni radona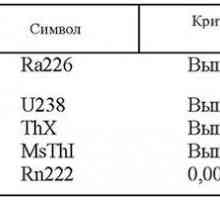 Prirodne radioaktivne vode
Prirodne radioaktivne vode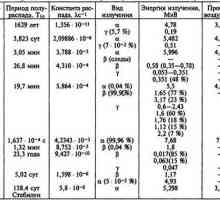 Svojstva broju izotopa radija
Svojstva broju izotopa radija Radioterapija ožiljaka
Radioterapija ožiljaka Utjecaj zračenja na ljudski životni vijek
Utjecaj zračenja na ljudski životni vijek Učinak zračenja na starenja i očekivanog trajanja života
Učinak zračenja na starenja i očekivanog trajanja života Liječenje Medicinski centar u UAE orthosports
Liječenje Medicinski centar u UAE orthosports Medicinska zakon: zakon, dokumenti, odgovornosti, pravila, zakoni.
Medicinska zakon: zakon, dokumenti, odgovornosti, pravila, zakoni. Medicinska zakon: zakon, dokumenti, odgovornosti, pravila, zakoni.
Medicinska zakon: zakon, dokumenti, odgovornosti, pravila, zakoni. Medicinska zakon: zakon, dokumenti, odgovornosti, pravila, zakoni.
Medicinska zakon: zakon, dokumenti, odgovornosti, pravila, zakoni. Učinak ionizirajućeg zračenja na štitnjače
Učinak ionizirajućeg zračenja na štitnjače
 Prirodne radioaktivne vode
Prirodne radioaktivne vode Radioterapija ožiljaka
Radioterapija ožiljaka Učinak ionizirajućeg zračenja na štitnjače
Učinak ionizirajućeg zračenja na štitnjače